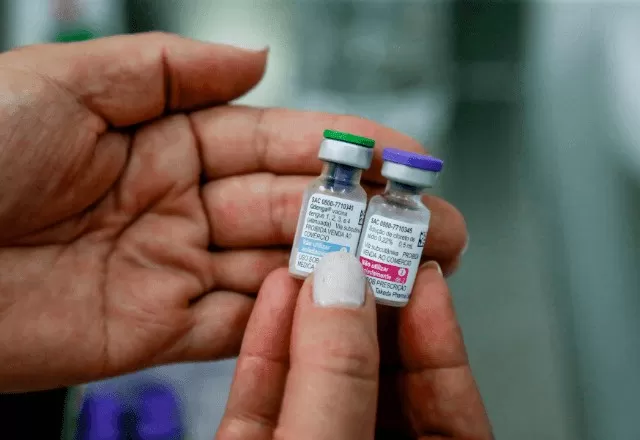
A Agência Nacional de Vigilância Sanitária (Anvisa) deve concluir, até o fim da próxima semana, a avaliação que pode levar à aprovação da vacina contra a dengue produzida pelo Instituto Butantan. O processo, classificado como prioritário pela agência, é considerado um passo decisivo no enfrentamento da doença no Brasil, que continua registrando altos índices de contaminação em várias regiões.
O diretor da Anvisa, Daniel Pereira, afirmou nesta sexta-feira (7) que a expectativa é finalizar a análise ainda na primeira quinzena de novembro. Ele explicou que o processo passou por uma etapa intensa de discussão técnica e que o comitê de especialistas da agência se reuniu recentemente para esclarecer as últimas dúvidas sobre o imunizante. “A vacina do Butantan é um processo prioritário para a agência. Tivemos muitas horas de avaliação técnica com apoio de especialistas externos e estamos próximos de uma conclusão”, declarou.
A nova vacina foi desenvolvida pelo Instituto Butantan, ligado ao governo de São Paulo, e é aguardada como uma alternativa nacional às vacinas importadas já aprovadas no Brasil. Até o momento, nenhum outro laboratório apresentou pedido de registro de imunizantes contra a dengue junto à Anvisa.
Durante a mesma coletiva, a diretoria da agência anunciou um conjunto de medidas para acelerar a tramitação de processos regulatórios, que atualmente somam cerca de 1,1 mil medicamentos sintéticos e 100 produtos biológicos aguardando análise. Entre as estratégias, está a adoção de ferramentas de inteligência artificial (IA), que devem reduzir em até 50% o tempo médio de avaliação de novos produtos.
O presidente da Anvisa, Leandro Safatle, explicou que o volume de pedidos de registro cresce cerca de 10% ao ano, o que sobrecarrega as equipes técnicas. “Estamos investindo em soluções que aumentem a produtividade e reduzam prazos. A inteligência artificial será uma aliada importante para otimizar análises e agilizar decisões sem comprometer a qualidade técnica”, afirmou.
Segundo Safatle, a meta é que, até dezembro de 2026, a agência consiga cumprir integralmente o prazo legal de um ano para a análise de novos registros. A Anvisa já conta com uma área interna dedicada ao desenvolvimento de ferramentas de IA, voltadas para triagem automatizada e organização de documentos técnicos.
Durante a reunião, o ministro da Saúde, Alexandre Padilha, participou por vídeo da África do Sul, onde representa o Brasil em um encontro de ministros da saúde do G20. Ele anunciou um aporte de R$ 25 milhões para fortalecer o uso de tecnologias digitais na Anvisa. “Esse investimento vai reduzir o tempo de análise, aumentar a qualidade técnica e permitir que novos medicamentos e vacinas cheguem mais rápido à população”, declarou.
Padilha também destacou parcerias com empresas da África do Sul e da Indonésia para acelerar o desenvolvimento e a produção de vacinas contra a tuberculose no Brasil, como parte da estratégia nacional de inovação em saúde.



Mín. 17° Máx. 26°